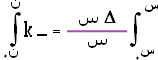|
|||||||||||||||||||||||
درس العلماء هذه التفاعلات وتوصلوا إلى مفهوم أسموه (عمر النصف) وهو يعني باختصار الزمن اللازم لتحول نصف المادة المتفاعلة ( وهي في مثالنا أعلاه A ) . دعنا نشتق علاقة زمن عمر النصف لتفاعل من الدرجة الأولى وهي علاقة يلزم لاشتقاقها إجراء عملية تكامل واستخدام للوغاريتمات الطبيعية أو ما يسمى اللوغاريتم النيبري Natural or Napierian Logarithm
ويرمز له عادة بالرمز ln ( وفي بعض الكتب العربية لط ) وأساس هذا اللوغاريتم هو العدد الذي يعطى في كتب الرياضيات الرمز e حيث
Logarithm الذي يرمز له عادة بالرمز log ( وفي بعض الكتب العربية لــو ) والذي أساسه هو العدد 10 . إن لــو 10 = 1 . ولكن لــط 10 =- 2.303 .
إذن عموماً ..........اللوغاريتم الطبيعي لأي عدد = اللوغاريتم العشري × 2.303 . فمثلاً لــط 100 = لـــو 100 × 2.303 = 2 × 2.303 = 4.606 . ونحن نستخدم عادة 2.3 بدلاً عن 2.303 لتسهيل العمليات والتخفيف من المنازل العشرية .
وهي معدل التغير في تركيز A بمرور الزمن (ن) أو السرعة = ثابت × تركيز A لنفرض أن التركيز الابتدائي لـ A = س0 وأن التركيز عند الزمن ن = س .
لط س ـ لط س0 = ـ k × ن ........................(1) |
|||||||||||||||||||||||
|
Copyright © 2001 - 2010 SchoolArabia. All rights reserved الحقوق القانونية وحقوق الملكية الفكرية محفوظة للمدرسة العربية |