سؤال
:
احسب قيمة PH
لمحلول
حمض HCl تركيزه 1.5 × 10-2
مول/لتر.
الجواب
:
1-
نكتب معادلة تأين الحمض HCl (قوي)
HCl
+
H2O " H3O+ +
Cl-
2- يكون
[H3O+] =
[HCl] =ه
1.5
× 10-2
مول/لتر.
3- نحسب PH .
PH
=
- لو [H3O+] =
- لو 1.5 ×
10-2 =
- (لو 1.5 + لو 10-2)
PH
=ه
2 – لو 1.5
(بما أن لو 1.5
= 0.18 من جداول
اللوغرتيمات)
إذاً PH
=ه
2 – 0.18 =
1.82.
سؤال
:
احسب قيمة
PH
لمحلول قاعدي Ca(OH)2 تركيزه (0.5 ×
10-3 مول/لتر).
الجواب
:
1- نكتب معادلة
التأين للقاعدة Ca(OH)2
(قوي).
Ca(OH)2 " Ca+2 +
2OH-
2- يكون
OH-]] =
2 × [Ca(OH)2] = 2
× (0.5 ×
10-3)
=
1 ×
10-3 مول / لتر .
3- نحسب [H3O+]
Kw
=
[OH-] [H3O+]
1 × 10-14
=
1 × 10-3 [H3O+]
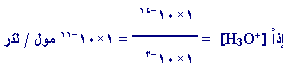
4- نحسب PH
PH
=
- لو [H3O+] = - لو 1 ×
10-11 =
- (لو1 + لو10-11)
PH
= 11
