عند إضافة ملح
NaCN
في الماء. ما التغيرات التي يمكن أن تحدث على قيمة PH؟
1- تعلم أن
الماء النقي وقبل أن يُضاف له الملح، يكون محلولاً متعادلاً
حيث
[-OH] =
[H3O+] =
11 × 10-7 مول/لتر أي تكون
PH
= 7
2-
وعند إضافة ملح
NaCN فإنه يتفكك
كلياً في الماء كما
يلي:
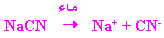
3-
وجود الشق
Na+
ليس له أي تأثير في قيمة PH
4-
الشق القاعدي للملح
هو –CN
(وهو قوي نسبياً) حيث أنه القاعدة المرافقة لحمض ضعيف
HCN.
وحيث أنه الشق الأقوى وهو قاعدي فهو يميل
لاستقبال بروتون من الماء كما
يلي:
(يحدث
تميّه)
OH - +
HCN D H2O
+
-CN
وهذا يعني تكوّن أيون الهيدروكسيد. وبالتالي زيادة
تركيزه في الماء مقارنة
بتركيز [H3O+] فترتفع قيمة PH
للمحلول، فتصبح أكبر من 7. (أي أن
المحلول قاعدي).
وبناء على ما
سبق:
| ملحوظة: يطلق على
تفاعل شقّي الملح او احداهما مع الماء بتمية
الملح
. |
سؤال :
محلول NaCN
في الماء قلوي التأثير. (فسِّر).
جواب: عند إضافة الملح للماء، فإنه
يتفكك كما يلي
:
-
CN
+ ®Na+ NaCN
أ- وجود
Na+
لا يؤثر في قيمة PH
ب- فيتفاعل الشق
القاعدي (القوي نسبياً) مع الماء كما يلي:
(يحدث
تميه)
CN- +
H2O D HCN +
OH-I
وهذا
يعني تكوّن
OH- وزيادة تركيزة عن تركيز
+ H3O
فيصبح المحلول قاعدياً
(قلوياً).
سؤال :
يحدث تميّه عند إضافة
ملح
NaCN إلى الماء.
(فسِّر ذلك).
جواب:
لأنه مع الماء يتفكك وتتفاعل أحد أيوناته مع
الماء كما يلي
:
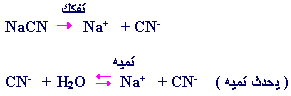
أَما Na+I فإنه لا يتفاعل مع الماء. (لا
يتميّه).
