|
الاتزان في محاليل القواعد الضعيفة(3)
|
|
مثال :
البيريدين C5H5N
قاعدة ضعيفة اكتشفت في قطران الفحم، فإذا علمت أن
Kb
= 1.5 × 10-9.
احسب PH لمحلول من البيريدين تركيزه
(0.1 مول/لتر). علماً بأن معادلة
التأين :
C5H5N + H2O D C5H5NH+ + OH-
جواب :
أ - نكتب معادلة التأين للقاعدة
الضعيفة
التراكيز
( مول / لتر ) |
C5H5N + H2O
D
C5H5NH+
+ OH - I |
| قبل التأين ( التفاعل ) |
صفر |
صفر |
( 0.01 ) |
| مقدار التغير |
( +
س ) |
( +
س ) |
( -
س ) |
| عند
الاتزان |
( س
) |
( س
) |
( 0.01 - س ) |
ب - بالتعويض في تعبير ثابت التأين
Kb

1.5 × 10-9 × 0.01 = س2
، وبأخذ الجذر التربيعي للطرفين
س= 3.87
× 10-6 مول/لتر، وبالتالي [OH-] = 3.87 × 10-6
مول/لتر
جـ - لحساب PH
لا بد من حساب [H3O+]
إذاً: Kw = [H3O+] [OH-]
1
× 10-14 =
[H3O+] (3.87
× 10-6)
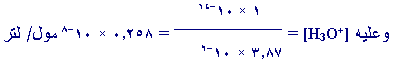
وبالتالي PH = - لو
[H3O+i ]
= - لو 0.258
× 10-8 = 8.6
سؤال :
احسب قيمة PH لمحلول قاعدة قوية صيغته الافتراضية
BOH وتركيزه
(0.01
مول / لتر)
|
|
