|
الفصل الرابع : الحسابات من
المعادلات الكيميائية (1)
|
 |
8. المعادلة : |
|
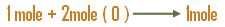 |
بأخذ عدد الجزيئات |
|
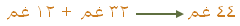 |
بأخذ الكتلة بالغرامات |
في هذه المعادلة الكيميائية كما في غيرها من المعادلات عدد
الذرات يبقى ثابتاً ( وبالتالي تبقى كتلتها ثابتة ) وهذا
يتوافق مع قانون حفظ المادة ( الكتلة ) ونصه :
لا تفنى الذرات ولا تستحدث في تفاعل كيميائي.
ـ كم غراماً
ينتج من غاز ثاني أوكسيد الكربون إذا تفاعل 3 غم من الكربون ؟
9. يتوافق أي تفاعل كيميائي مع قانون حفظ المادة ، ولذلك يجب
أن يكون عدد الذرات في طرفيها متساو وبالتالي كتلتها متساوية .
|
 |
يحترق غاز الميثان في الأوكسجين حسب المعادلة : |
هذا الشكل من المعادلة غير متزن لأن عدد ذرات الأوكسجين
والهيدروجين غير متساوٍ في الطرفين ، تأكد من ذلك . لا يتوافق
هذا الأمر مع قانون حفظ الكتلة ، إذن علينا أن نساوي عدد
الذرات في الطرفين مع المحافظة على هوية المواد الداخلة في
التفاعل والناتجة عنه وعدم التغيير في الصيغ والرموز ؟
|
 |
كيف يتم لنا ذلك ؟
يتم عن طريق الضرب بأرقام مناسبة |
اعتمد على المعادلة الموزونة في إجابتك عن السؤال التالي :
ـ كم عدد
مولات الماء التي تنتج عن احتراق مول واحد من الميثان ؟
إجابة السؤال
|

