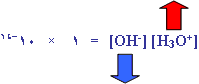|
 التأين الذاتي للماء
:
التأين الذاتي للماء
:
ثبت عملياً أن الماء النقي يوصل التيار الكهربائي بدرجة
ضعيفة، وهذا يدل على وجود أيونات موجبة وأخرى سالبة مسؤولة عن ذلك. إن مصدر هذه
الأيونات هو التأين الذاتي للماء حيث يمكن لجزيء ماء أن يمنح بروتوناً لجزيء
ماء آخر.
وبما أن التوصيل الكهربائي للماء النقي ضعيف، لذا فإن
تركيز أيوني
+H3O
،ه-OH
قليل جداً مقارنة بتركيز الماء، وعليه فإن تركيز الماء لا يحصل عليه تغيير يذكر
بفعل التأين الذاتي للماء ، ولذلك فإن :
[H2O]2
= مقدار ثابت
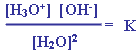
ويصبح تعبير ثابت الاتزان على النحو :
K
× [H2O]2
= [H3O+]
[OH-]
وإذا عبرنا عن المقدار (K
×
[H2O]2
) بالمقدار الثابت Kw
فإن :
Kw
: ثابت تأين الماء = 1 × 10-14 عند درجة 25ْ س.
 حساب
[H3O+]
و
[OH-]
في الماء النقي
حساب
[H3O+]
و
[OH-]
في الماء النقي
إن التأين الذاتي للماء يعطي تراكيز متساوية من أيونات
+H3O
،ه-OH
بما أن :
|
[OH-] [H3O+]
= Kw |
|
=
[H3O+]
[H3O+] لأن [H3O+]
= [OH-] |
|
2 |
=
[H3O+] |
|
 |
 أثر إضافة
حمض أو قاعدة للماء النقي
أثر إضافة
حمض أو قاعدة للماء النقي
في
الماء النقي يكون
[OH-]
=
[H3O+]
=
1 × 10-7 مول/لتر وفي هذه الحالة يكون الماء
متعادلاً.
إضافة
حمض إلى الماء يزيد من
[H3O+]ويقلل
من
[OH-]
مع بقاء قيمة
Kw
ثابتة.
|
1 × 10-7 مول/لتر. |
> |
[+H3O] |
وفي هذه
الحالة يكون المحلول حمضياً لأن |
إضافة قاعدة إلى الماء يزيد من
[OH-]
ويقلل من
[H3O+]
مع بقاء قيمة
Kw
ثابتة.
|
1 × 10-7 مول/لتر. |
> |
[-OH]
|
وفي هذه
الحالة يكون المحلول حمضياً لأن |
|