|
الحسابات الكيميائية
Stoichiometry
الفصل الثالث : الحسابات
المبنية على الصيغ
19. حللت عينة مقدارها 1.5 غم من مركب فوجد أنها تتكون من
0.6غم كربون ، 0.1 غم هيدروجين ، والباقي أوكسجين ، أوجد
الصيغة البسيطة للمركب . أوجد أيضاً الصيغة الجزيئية للمركب
إذا كان وزن المول منها = 120 غم .
تحليل السؤال :
ـ
كم وزن الأوكسجين في العينة = 1.5 ـ 0.6 ـ 0.1 =
0.8 غم .
ـ العينة معطاة بالغرامات وحتى تكتب
الصيغة يجب أن نحول الغرامات إلى
-----------.
إذن صيغة المركب حسب هذه الأرقام هي
----------------
.
وحتى نحول هذه الأعداد إلى أعداد صحيحة
نقسم على -------------
.
ـ
إذن الصيغة البسيطة =
CH2O.
ـ ما كتلة المول من الصيغة البسيطة = ( 1 × 12 ) + ( 2 ×
1) + ( 1 × 16)
= 12 + 2 + 16
= 30 غم .
ـ ولكن كتلة مول من الصيغة الجزيئية = 120 غم .
|
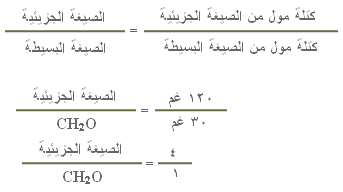 |
ولكن ... |
إذن الصيغة الجزيئية = 4 ×
CH2O
=
----------------
.
إجابة السؤال
|

