|
المنهاج الأردني |
الثانوية العامة
(الثاني الثانوي العلمي)
|
|
امتحان شهادة الدراسة
الثانوية العامة لعام 2001 |
 السؤال
الثالث :
السؤال
الثالث :
يتضمن الجدول الآتي رموزاً وصيغاً كيميائية لعدد من
المواد الصلبة :
|
29Cu |
CsCl |
SiO2
كوارتز |
CHCl3 |
|
30Zn |
SiO2
( في الزجاج العادي ) |
6C
غرافيت |
I2 |
انقل
إلى دفتر إجابتك من الجدول السابق الرمز أو الصيغة الكيميائية التي تمثل مادة :
1. جزيئية غير
بلورية .
2. جزيئية بلورية
قطبية غير موصلة للتيار الكهربائي في الحالة الصلبة .
3. بلورية ترتبط
جزيئاتها بترابط تساهمي شبكي .
4. فلزية بلورية لا تحتوي ذراتها على الكترونات منفردة .
5.
بلورية غير قطبية ترتبط جزيئاتها بقوى لندن.
6. بلورية سوداء نسبياً وموصلة للتيار الكهربائي.
إجابة السؤال
 السؤال الرابع :
السؤال الرابع :
|
المعلومات |
صيغةالحمض |
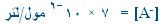 |
HA |
|
 |
HB |
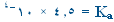 |
HC |
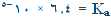 |
HD |
|
أ)
لديك أربعة محاليل مائية لبعض الحموض الضعيفة بتراكيز متساوية (0.1 مول
/ لتر ) لكل منها .
بالإعتماد على المعلومات الواردة عن كل حمض في الجدول المجاور , أجب
عما يأتي :
1. احسب قيمة
Ka
لكل من الحمضين :
HB , HA. |
2. أي
القاعدتين المرافقتين أقوى :
C-
أم
D-؟
3.
اكتب معادلة تفاعل الحمض
HC(aq)
مع القاعدة
NH3(aq)
, وفق تعريف برونستد ـ لوري , وحدد الزوجين المرافقين من الحمض والقاعدة في
معادلة التفاعل نفسه .
4.
ماذا يحدث لقيمة
pH
للحمض
HB(aq)
إذا خففنا التركيز إلى 0.05 مول / لتر .
( تقل , تبقى ثابتة , تزداد) ؟
ب)
تم تحضير محلول من الحمض H2CO3
والملح NaHCO3
بالتركيز نفسه .
فإذا
كان [H3O+]
في المحلول = 4 × 10-7 مول / لتر , ويتأين الحمض في الماء كما في
المعادلة الآتية :
1.
احسب قيمة ثابت التأين Ka
للحمض H2CO3
.
2. اكتب صيغة الأيون المشترك.
|
لتصبح قيمة
pH
للمحلول تساوي 7.4 وهي القيمة المناسبة |
 |
احسب قيمة النسبة : |
3. |
ليؤدي الدم وظيفته في الجسم (
علماً بأن لو 4 = 0.6).
إجابة السؤال