|
الفصل الرابع : الحسابات من
المعادلات الكيميائية (1)
إجابة أسئلة الاختبار القبلي /
البعدي :
7.توزع
العلامات على الخطوات كما هو ظاهر على اليمين :
تحليل السؤال :
وهكذا فإن العلاقة هي أن كل مولين من نيترات الفضة تعطي مولاً
واحداً من اليود ، وما علينا الآن سوى أن نحول المولات إلى
غرامات .
|
= ( 1 × 108 غم ) + ( 1 × 14 غم ) + ( 3 × 16 غم ) |
AgNO3 |
مول من نيترات الفضة
|
|
= 108 غم + 14 غم + 48 غم = 170 غم
|
|
|
2 مول من نيترات الفضة = 2 × 170 = 340 غم
|
= 2 × 127 غم = 254 غم |
I2
|
مول من |
إذن....
|
254 غم يود |
ـ |
AgNO3
|
340
غم من
|
|
1 غم يود |
ـ |
؟؟؟؟؟ |
|
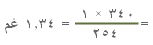 |
وزن نيترات الفضة اللازم لإنتاج غرم واحد من اليود
|
|

