|
|
خلايا التحليل الكهربائي |
 |
|
4. |
يحدث اختزال
للأيون الموجب على المهبط . |
|
يتجه أيون الصوديوم إلى المهبط ويحدث له اختزال بفعل الإلكترونات
القادمة من البطارية ويتجمع على المهبط . |
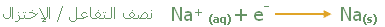 |
|
5. يحدث
تأكسد للأيون السالب على المصعد . |
|
يتجه أيون
الكلوريد إلى المصعد ويحدث له تأكسد , وتتحد كل ذرتين منها لتكون
جزيئاً من جزيئات الكلور , وتتصاعد على المصعد. |
|
 |
|
6. |
تخرج الإلكترونات
من المصعد لتعود إلى البطارية ثانية وتكمل دورتها . |
|
لذا تكون
التفاعلات التي تحدث على كل قطب : |
|
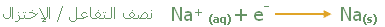 |
|
 |
|
ولمعرفة
التفاعل الخلوي , وجهد الخلية , نستخرج قيم جهود الإختزال من
السلسلة الكهركيميائية . |
|
|
|
وبضرب نصف تفاعل الإختزال في
(2) , وجمع نصفي التفاعل نحصل على معادلة التفاعل الخلوي . |
|
 |
|
 |
|
 |
|
 |
|
وتكون نواتج التحليل الكهربائي
: |
|
1. |
تصاعد
غاز الكلور على المصعد . |
|
2. |
تكون
الصوديوم على المهبط . |
|
لاحظ أن إشارة جهد
التفاعل (ْE)
سالبة , وهذا يعني أن التفاعل غير تلقائي , ولا يمكن حدوثه إلا
بتزويد التفاعل بفرق جهد يزيد عن 4.07 فولت . |
|
تدريب : |
|
أكتب المعادلات
التي تحدث على المصعد والمهبط عند تحليل مصهور بروميد الكالسيوم
CaBr2 كهربائياً باستخدام أقطاب من البلاتين , إذا علمت
أن : |
|
 |
|
 |
|
|

