تمرين (1) : أكمل الفراغ في العبارتين التاليتين :
أ- العدد الموضوع اسفل رمز العنصر والى يساره هو عدده الذري
وهو عدد ــــ الموجودة في نواة ذرته .
ب- العدد الموضوع أعلى رمز العنصر والى يساره وهو العدد الكتلي
وهو مجموع عدد ــــ
و ــــــ في نواة ذرته .
تمرين (2) : أكمل الجدول التالي مستعيناً
بالجدول الدوري :
|
اسم العنصر
|
رمزه
|
عدده الذري
|
عدده الكتلي
|
|
الكبريت
|
|
|
|
|
|
|
i53
|
|
|
|
|
|
i23
|
|
القصدير
|
|
|
|
|
|
|
|
|
|
|
Zn
|
|
ا |
تمرين (3) : اكمل
الجدول التالي :
|
رمز العنصر
|
عدد البروتونات
|
عدد النيوترونات
|
رمز العنصر
|
عدد البروتونات
|
عدد النيوترونات
|
|
I199F
|
|
|
I3517Cl
|
|
|
|
I4018Ar
|
|
|
I5224Cr
|
|
|
|
I20080Hg
|
|
|
I2412Mg
|
|
|
تمرين (4)
:
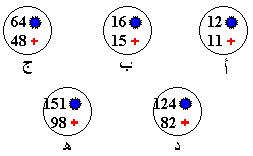
الأشكال التالية تمثل انوية ذرات :
حدد العدد الذري والعدد الكتلي وعدد الإلكترونات لكل ذرة منها
في حالة التعادل .
لمعرفة
الاجابات اضغغط هنا
