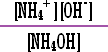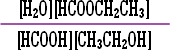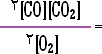|
||||||||||||||||||||
1..............
3. ملاحظة : المعادلة غير موزونة زنها أولاً .
4.................
6. 7. 8. ملاحظة : زن المعادلة أولاً .
1. أ. يقلل من تركيز CO لأن التفاعل يتجه إلى اليمين حيث الجهة التي ينقص فيها عدد المولات ( لاحظ أن مولات C(s) تعتبر ثابتة ، لماذا ؟). تذكر جيداً أن حجم المولات الغازية يتناسب مع عددها ( راجع قانون أفوجادرو ) . ب. لا يؤثر على تركيز CO لأنه لا يغير حالة الاتزان ، لماذا ؟ .
هذا السلوك يؤدي إلى رفع تركيز Br-
3. ينخفض تركيز أيون الهيدرونيوم ، فسر صحة هذه الإجابة بنفسك . 4. 5. أ. ب. تخفيض الضغط يؤدي إلى زيادة الحجم لذلك تزداد سرعة التفاعل العكسي لحين حدوث اتزان جديد . إذن ينخفض تركيز غاز الأوكسيجين .
|
||||||||||||||||||||
|
Copyright © 2001 - 2010 SchoolArabia. All rights reserved الحقوق القانونية وحقوق الملكية الفكرية محفوظة للمدرسة العربية |