|
|
|
الترابط بين الجزيئات وحالات المادة |
|
|
|
إجابات الاختبار القبلي
|
1)
كل مادة موضوعة في العمود الصحيح الخاص
بها تأخذ علامة واحدة :
|
مواد تربط بين
جزيئاتها قوى فان ديرفال ( لندن) |
مواد تربط بين
جزيئاتها رابطة هيدروجينية |
مواد تربط بين
جزيئاتها روابط
ثنائية القطب |
|
CH4 |
HF |
HCl |
|
BF3 |
CH3CH2CH2CH2OH |
HBr |
|
Br2 |
CH3CH2NH2 |
OF2 |
|
Kr |
|
H2S |
|
SiCl2 |
|
NO |
|
CH3CH2CH3 |
|
ICl |
|
|
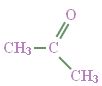 |
 |
رجوع
2)
المادة السائلة هي
CH3OH
( علامة واحدة )
ترتبط جزيئات هذه المادة مع بعضها بروابط
هيدروجينية قوية.
( علامتان )
في الجزيئات الأخرى الروابط هي قوى فان ديرفال
الضعيفة.
( علامتان )
رجوع
3)
|
 |
|
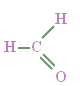
تمثل الرابطة الهيدروجينية (بالشكل ـ ـ ـ ـ ـ ـ
) التي تعمل كجسر يربط بين الجزيئين. |
إذار رسمت بطريقة صحيحة
تأخذ ( 5 علامات )
رجوع
4)
يستطيع كل مركب من
المركبين تكوين روابط هيدروجينية لوجود ذرة النيتروجين (
صغيرة الحجم وعالية الكهروسلبية ) ,ولكن المركب الأول
NH2CH2CH2NH2
يحوي مجموعتين من (NH2) في حين
أن المركب الثاني
CH3CH2CH2NH2 يحوي
مجموعة واحدة من (NH2) , لذلك
فالمركب الأول يستطيع أن يكوّن من الروابط الهيدروجينية
مثلي ما يكونه المركب الثاني , وبذلك تكون قوة الترابط بين
جزيئات المركب الأول أكبر , ولفصلها وإضعاف الروابط تحتاج
لحرارة أكبر لذلك فإن درجة غليانه أعلى . إليك شكلاً يوضح
كيف تحث الروابط الهيدروجينية وعددها في كلا المركبين :
 |
المركب الأول: |
 |
المركب الثاني : |
النقط تمثل الروابط الهيدروجينية , وبالطبع يرتبط النيتروجين
بهيدروجين جزيء آخر , والهيدروجين بنيتروجين الجزيء الآخر
فتنشأ شبكة معقدة من الروابط الهيدروجينية ترفع درجة الغليان ,
ولكنها تكون أعقد في حالة المركب الأول , لذلك فإن درجة غليانه
أعلى.
توزع العلامة كما يلي :
1. معرفة أن الرابطة هيدروجينية والتفسير الخاص بتكونها
(4) علامات
.
2. معرفة أن عدد روابط المركب الأول مثلي الثاني
( 4) علامات .
3. وجود روابط هيدروجينية أكثر يعني درجة غليان أعلى
(2) علامتان .
رجوع